Роль эпигенетических механизмов в развитии дегенеративных заболеваний — понимание взаимосвязи генетики и окружающей среды для прогнозирования и предотвращения нарушений здоровья
Contents
- 1 Механизмы эпигенетики и их воздействие на генетическую экспрессию
- 2 Влияние эпигенетики на развитие раковых заболеваний
- 3 Связь эпигенетики с возникновением болезни Альцгеймера
- 4 Связь между эпигенетикой и развитием болезни Паркинсона
- 5 Влияние эпигенетических факторов на здоровье сердца
- 6 Взаимосвязь эпигенетики и развития диабета
- 7 Эпигенетика и ее влияние на заболевания сердца
- 8 Импакт эпигенетики на механизмы возникновения дегенеративных заболеваний
- 9 Вопрос-ответ:
- 9.1 Что такое эпигенетические механизмы?
- 9.2 Как эпигенетические механизмы связаны с дегенеративными заболеваниями?
- 9.3 Могут ли эпигенетические механизмы быть наследуемыми?
- 9.4 Какие факторы могут влиять на эпигенетические механизмы?
- 9.5 Можно ли воздействовать на эпигенетические механизмы для предотвращения дегенеративных заболеваний?
- 9.6 Какие эпигенетические механизмы могут влиять на развитие дегенеративных заболеваний?
- 9.7 Какие дегенеративные заболевания могут быть связаны с эпигенетическими механизмами?
- 9.8 Можно ли изменить эпигенетические механизмы в организме и предотвратить развитие дегенеративных заболеваний?
- 9.9 Какие другие факторы, помимо эпигенетических механизмов, могут влиять на развитие дегенеративных заболеваний?
- 10 Видео:
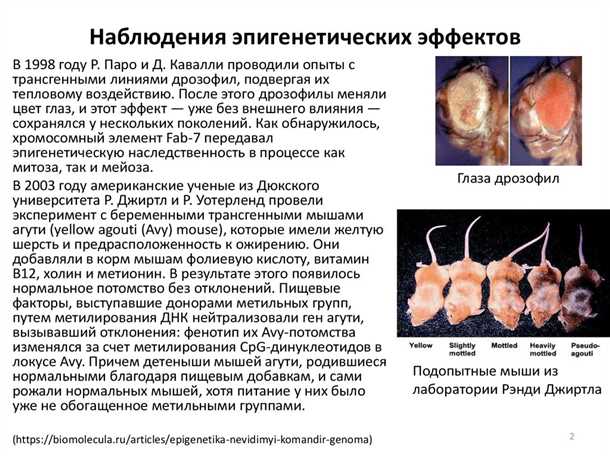
Весьма удивительно, как ряд химических модификаций ДНК и гистонов может оказывать значительное влияние на наш организм, способствуя формированию различных заболеваний. Так называемые эпигенетические механизмы играют важную роль в патогенезе дегенеративных состояний, которые становятся все более распространенными в современном обществе.
Закодированные в геноме изменения, которые не затрагивают саму последовательность нуклеотидов ДНК, а скорее связаны с ее измененной доступностью для транскрипции, являются главными игроками в эпигенетических процессах. Один из наиболее известных механизмов — метилирование ДНК, влияющее на активность генов посредством добавления метильных групп к щелочным остаткам. Другой ключевой эпигенетический механизм — модификация хвостовых гистоновых белков. Они обусловливают компактность хроматина и, тем самым, преграждают путь к определенным генам.
Хотя все эти изменения, происходящие на уровне ДНК и хроматина, могут быть перенесены от одного поколения к другому, они, тем не менее, являются обратимыми и могут быть влиянием факторов окружающей среды. Благодаря этой гибкости, эпигенетические механизмы становятся центром внимания исследователей, связанных с патогенезом различных дегенеративных заболеваний. Понимание взаимосвязи между этими механизмами и патологическими состояниями может открыть новые возможности для разработки инновационных способов профилактики и лечения этих заболеваний.
Механизмы эпигенетики и их воздействие на генетическую экспрессию
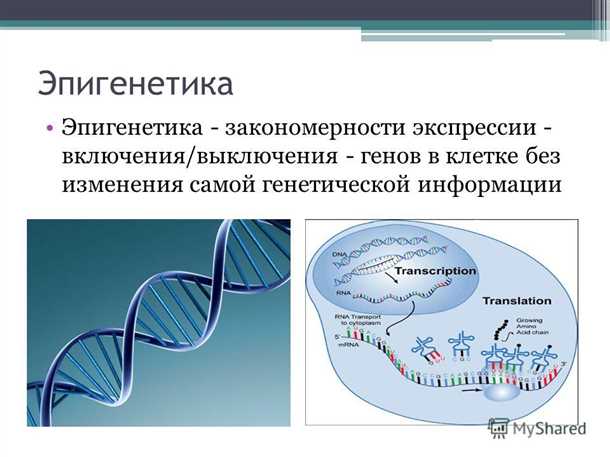
Один из основных механизмов эпигенетики — метилирование ДНК. В процессе метилирования к определенным участкам ДНК прикрепляются метильные группы, что может блокировать активность соответствующих генов. Таким образом, метилирование ДНК играет ключевую роль в регуляции генетической экспрессии.
Другим важным механизмом эпигенетики является модификация гистонов. Гистоны — это белки, вокруг которых обвивается ДНК, формируя хроматиновую структуру. Модификация гистонов может влиять на доступность генов для транскрипции. Например, ацетилирование гистонов облегчает доступ транскрипционных факторов к генам, что способствует их активации.
Также эпигенетические изменения могут происходить на уровне РНК. Например, метилирование или деметилирование рибонуклеиновой кислоты (РНК) может влиять на стабильность и функциональность транскриптов, что в конечном итоге определяет активность определенных генов.
Осознание роли эпигенетических механизмов в генетической регуляции открывает новые перспективы в исследовании и лечении различных дегенеративных заболеваний. Понимание, какие механизмы эпигенетики могут быть нарушены при определенных патологиях, позволяет разрабатывать новые подходы к лечению, направленные на нормализацию эпигенетических изменений и восстановление нормального функционирования генов.
Влияние эпигенетики на развитие раковых заболеваний

Эпигенетика – это область науки, изучающая изменения в генетической экспрессии без изменения самой последовательности ДНК. Эти изменения могут быть вызваны внешними факторами, такими как питание, окружающая среда или стресс. Они могут приводить к неправильному включению или отключению генов, что в итоге может привести к развитию раковых клеток и формированию опухолей.
Механизмы эпигенетики играют важную роль в возникновении раковых заболеваний. Они могут изменять активность определенных генов, что может приводить к нарушению процессов роста, развития и регуляции клеток. Неконтролируемое деление клеток, аномальный рост и образование опухолей – все это связано с нарушениями в эпигенетических механизмах.
Одним из распространенных эпигенетических изменений при раке является метилирование ДНК. Это процесс, в котором метильные группы добавляются к ДНК, что может повлиять на ее активность. Метилирование генов, контролирующих рост и развитие клеток, может привести к неоднократному делению клеток и образованию опухолей.
Кроме того, эпигенетические механизмы могут влиять на активность генов, ответственных за ремонт ДНК и контроль над циклом клеточного деления. Неконтролируемое деление клеток и нарушение процессов ремонта ДНК могут способствовать развитию рака.
Понимание роли эпигенетики в развитии рака открывает новые возможности для предотвращения, диагностики и лечения этого опасного заболевания. Изучение эпигенетических механизмов может помочь выявить ранние признаки рака и разработать инновационные методы лечения, основанные на управлении генетической экспрессией и эпигенетических изменениях.
Связь эпигенетики с возникновением болезни Альцгеймера

Сегодня уже известно, что эпигенетические изменения в геноме могут участвовать в формировании первоначальных стадий болезни Альцгеймера. Эти изменения происходят в клетках головного мозга и приводят к нарушениям в работе нейронов, межсинаптической связи и синаптическим дефектам. Подобные нарушения проявляются в активации патологических белковых агрегатов, таких как бета-амилоидные и тау-белки, которые отвечают за образование амилоидных пластинок и неврофибриллярных узлов.
Изучение эпигенетических механизмов в развитии болезни Альцгеймера позволяет понять причины ее возникновения и прогрессирования. Например, гипометилирование ДНК в определенных областях генома может привести к активации экспрессии генов, связанных с воспалением или стрессовыми ответами клетки, что в конечном итоге приводит к повышенной продукции бета-амилоидных белков и ускоренному старению нейронов. Одновременно, гиперметилирование ДНК может подавлять экспрессию генов, отвечающих за обновление и восстановление нервных клеток, что препятствует нормальной работе мозга и вызывает прогрессию болезни.
Учитывая огромное значение эпигенетических факторов в развитии болезни Альцгеймера, открываются новые перспективы для создания инновационных подходов в диагностике и лечении этого заболевания. Исследование и модификация эпигенетических механизмов могут сыграть ключевую роль в разработке новых лекарственных препаратов и терапевтических методик, направленных на предотвращение или замедление прогрессирования болезни.
Связь между эпигенетикой и развитием болезни Паркинсона
Влияние метилирования ДНК на развитие болезни Паркинсона
Одним из эпигенетических механизмов, который значительно влияет на развитие болезни Паркинсона, является метилирование ДНК. Метилирование происходит путем добавления метильной группы к цитозиновым основаниям в генном коде и может привести к инактивации определенных генов, что может иметь негативное влияние на функционирование клеток и их выживаемость в областях мозга, ответственных за координацию движения.
Исследования показывают, что у пациентов с болезнью Паркинсона происходит гиперметилирование определенных генов, что приводит к их инактивации. В результате этого процесса, снижается уровень экспрессии белков, ответственных за поддержание здорового функционирования клеток мозга, что может способствовать прогрессии заболевания.
Влияние модификации гистонов на развитие болезни Паркинсона
Кроме метилирования ДНК, модификация гистонов – белковых структур, которые образуют хроматиновую структуру ДНК, также играет важную роль в развитии болезни Паркинсона. Различные модификации гистонов, такие как ацетилирование, метилирование, фосфорилирование, могут влиять на доступность генов для транскрипции и, следовательно, на экспрессию белков.
Недавние исследования показали, что определенные модификации гистонов в мозге пациентов с болезнью Паркинсона отличаются от нормальных образцов. Например, наблюдалось увеличение уровня метилирования и дефицит ацетилирования гистонов в генах, ответственных за митохондриальную функцию и цикл сна-бодрствования. Это может свидетельствовать о негативном влиянии на энергетические процессы в клетках мозга, а также на баланс между сном и бодрствованием, что характерно для пациентов с болезнью Паркинсона.
В целом, понимание влияния эпигенетических механизмов на развитие болезни Паркинсона открывает новые перспективы для разработки эффективных методов диагностики, профилактики и лечения этого неврологического заболевания.
Влияние эпигенетических факторов на здоровье сердца
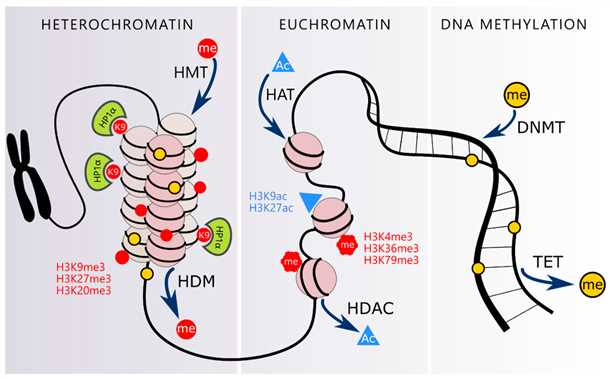
Один из важных механизмов эпигенетических изменений, связанных с сердечной патологией, – это метилирование ДНК. Метилирование является процессом добавления групп метиловых (CH3) на ДНК-молекулу, что часто приводит к подавлению экспрессии генов. В случае сердечных заболеваний, относительное увеличение метилирования определенных генов может стать фактором риска или способствовать прогрессированию болезни.
Влияние гистоновых модификаций на заболевания сердца
Кроме метилирования ДНК, эпигенетические изменения также могут быть связаны с модификациями гистонов – белковых комплексов, вокруг которых образуется ДНК. Гистоновые модификации, например, ацетилирование или метилирование гистонов, могут влиять на уровень компактности хроматина и, соответственно, на доступность генов для транскрипции. Изменения в гистоновых модификациях могут быть связаны с развитием сердечной патологии и его прогрессией.
Другим важным фактором риска для сердечно-сосудистых заболеваний является окружающая среда. Эпигенетические изменения могут быть вызваны факторами внешней среды, такими как питание, физическая активность, стресс и токсические вещества. Например, плохое питание или недостаток физической активности могут привести к изменениям в экспрессии генов, связанных с сердечной патологией.
Итоги и перспективы
Исследование эпигенетических факторов, влияющих на заболевания сердца, позволяет лучше понять механизмы развития и прогрессирования сердечной патологии. Открывая новые пути для диагностики и лечения, эпигенетика может стать важным инструментом в борьбе с сердечными заболеваниями в будущем. Дальнейшие исследования позволят более точно определить эпигенетические механизмы, связанные с развитием сердечно-сосудистых заболеваний, и разработать персонализированный подход к предупреждению и лечению этих заболеваний.
Взаимосвязь эпигенетики и развития диабета
Эпигенетика, одна из важных областей научных исследований, оказывает значительное влияние на развитие различных заболеваний, включая дегенеративные, такие как диабет. Возможность изменения генетической экспрессии без изменения самой ДНК стала объектом интереса ученых, ирисрующих наши представления о наследственности и влиянии окружающей среды на наш организм.
Когда речь идет о развитии диабета, эпигенетические факторы могут играть важную роль в патогенезе и прогрессии заболевания. Несмотря на то, что наследование генетической предрасположенности для диабета может быть важным фактором, эпигенетические изменения также оказывают влияние на развитие и течение заболевания. Они могут нарушать нормальное функционирование поджелудочной железы и клеток, отвечающих за выработку инсулина, что приводит к развитию диабета.
Эпигенетические модификации, такие как метилирование ДНК, модификация гистонов и некодирующие РНК, могут изменять активность генов, связанных с метаболизмом глюкозы и инсулином. Они влияют на способность организма усваивать глюкозу из крови и эффективно использовать инсулин, регулируя уровень сахара в крови.
Исследования показывают, что эпигенетические изменения, происходящие в раннем детстве, могут оказывать долгосрочное влияние на риск развития диабета в будущем. Факторы, такие как питание матери во время беременности, а также диета и образ жизни в детстве, могут оказывать эпигенетическое воздействие на гены, связанные с регуляцией уровня глюкозы.
Дальнейшие исследования эпигенетических механизмов, взаимодействующих с различными генами, связанными с диабетом, могут пролить свет на патогенез этого заболевания и помочь развить новые методы диагностики и лечения. Понимание взаимосвязи между эпигенетикой и диабетом может открыть новые перспективы для предотвращения и эффективного контроля данного заболевания.
Эпигенетика и ее влияние на заболевания сердца
1. Влияние эпигенетических механизмов на генетическую экспрессию
Генетическая экспрессия, то есть процесс, по которому гены в нашем организме активируются или отключаются, является фундаментальной основой для нормального функционирования организма. Эпигенетика изучает изменения в генетической экспрессии, которые не связаны с изменением ДНК-последовательности. Такие изменения могут произойти под влиянием факторов окружающей среды, образа жизни, пищевых привычек, а также генетических мутаций.
2. Роль эпигенетики в развитии заболеваний сердца
Накопившиеся данные свидетельствуют о том, что эпигенетические изменения могут оказывать существенное влияние на развитие сердечно-сосудистых заболеваний. Например, группы исследователей обнаружили изменения в активации генов, ответственных за воспаление и окислительный стресс, что может привести к развитию атеросклероза и других сердечно-сосудистых осложнений.
- Индивидуальные факторы – образ жизни, пищевые привычки, стресс.
- Влияние генов – генетические мутации могут привести к системным изменениям в генетической экспрессии, которые в свою очередь могут быть связаны с возникновением сердечно-сосудистых заболеваний.
- Взаимодействие с окружающей средой – воздействие токсических веществ, загрязнение воздуха, уровни шума и других факторов окружающей среды могут вызывать эпигенетические изменения, которые повышают риск развития заболеваний сердца.
3. Возможности использования эпигенетических механизмов для предотвращения и лечения сердечно-сосудистых заболеваний
Проведенные исследования показывают, что эпигенетика может быть потенциальной мишенью для разработки новых лекарственных средств и терапевтических подходов. Разработаны экспериментальные методы регуляции генетической экспрессии с использованием эпигенетических модификаций, которые направлены на восстановление нормального функционирования сердечно-сосудистой системы.
Импакт эпигенетики на механизмы возникновения дегенеративных заболеваний
Различные исследования показывают, что эпигенетические факторы могут значительно влиять на развитие раковых заболеваний. Некоторые из этих факторов могут быть связаны с наследственностью, однако большую роль играют изменения, возникающие во время жизни. Эти изменения могут быть причиной мутаций в генах, что в свою очередь способствует развитию рака. Исследования показывают, что некоторые эпигенетические модификации могут быть обратимыми, что открывает перспективы для новых методов лечения этой опасной болезни.
Болезнь Альцгеймера — одно из самых распространенных неврологических заболеваний, причины которого до сих пор не полностью изучены. Однако эпигенетика может сыграть важную роль в объяснении механизмов возникновения и развития этого заболевания. Исследования выявили связь между определенными эпигенетическими изменениями и ухудшением памяти и когнитивных функций, которые являются основными симптомами Альцгеймера. Это открывает перспективы для разработки новых методов предотвращения и лечения болезни.
Связь между эпигенетикой и развитием болезни Паркинсона также была обнаружена. Некоторые исследования показывают, что эпигенетические изменения влияют на экспрессию генов, связанных с нейродегенерацией, характерной для этого заболевания. Однако механизмы, через которые эти изменения происходят, до сих пор подробно не изучены. Это представляет интерес для дальнейших исследований и может привести к новым подходам в лечении и профилактике заболевания Паркинсона.
Эпигенетические факторы также могут оказывать влияние на развитие болезни сердца. Изменения в экспрессии генов, вызываемые эпигенетическими механизмами, могут быть связаны с различными факторами риска, такими как курение, повышенное потребление алкоголя и неправильное питание. Понимание этих механизмов может помочь в разработке новых подходов к лечению и профилактике сердечно-сосудистых заболеваний.
Исследования также показывают связь между эпигенетикой и развитием диабета. Эпигенетические изменения могут влиять на функцию и экспрессию генов, связанных с обработкой глюкозы и инсулинорезистентностью. Это может привести к развитию диабета и его осложнений. Понимание этих механизмов может быть полезным для разработки новых методов профилактики и лечения этого распространенного заболевания.
Быстрый прогресс в исследованиях эпигенетических механизмов открывает новые перспективы в лечении и профилактике различных дегенеративных заболеваний. Понимание связей между эпигенетикой и развитием этих заболеваний может помочь в разработке инновационных методов лечения и предотвращения, что делает эпигенетику одной из наиболее перспективных областей медицины.
Вопрос-ответ:
Что такое эпигенетические механизмы?
Как эпигенетические механизмы связаны с дегенеративными заболеваниями?
Могут ли эпигенетические механизмы быть наследуемыми?
Какие факторы могут влиять на эпигенетические механизмы?
Можно ли воздействовать на эпигенетические механизмы для предотвращения дегенеративных заболеваний?
Какие эпигенетические механизмы могут влиять на развитие дегенеративных заболеваний?
Какие дегенеративные заболевания могут быть связаны с эпигенетическими механизмами?
Можно ли изменить эпигенетические механизмы в организме и предотвратить развитие дегенеративных заболеваний?
Какие другие факторы, помимо эпигенетических механизмов, могут влиять на развитие дегенеративных заболеваний?
Видео:
Суперспособности и лечение рака: сможет ли человечество управлять генами? / Сергей Киселев
Что такое эпигенетический откат? Рассказывает Юрий Дейгин.







