Эпигенетика — ключевая роль в понимании механизмов возникновения и развития неврологических заболеваний
Contents
- 1 Влияние механизмов эпигенетики на развитие патологических состояний В данном разделе статьи мы рассмотрим, как изменения в механизмах эпигенетики оказывают влияние на формирование и развитие различных патологических состояний, связанных с функционированием нервной системы. Первое, на что мы обратим внимание, — это эффект эпигенетических изменений на активность генов, которые отвечают за работу нервных клеток и межклеточную коммуникацию. Изучение этих изменений позволяет лучше понять, какие механизмы лежат в основе возникновения неврологических патологий. Далее, мы рассмотрим влияние химических метиловых групп на генетическую активность и, соответственно, на функционирование нервной системы. Эти изменения могут быть вызваны как внешними факторами, такими как стресс или воздействие токсических веществ, так и внутренними факторами, такими как генетические предрасположенности. Особым вниманием мы обратимся к роли эпигенетических механизмов в создании «памяти» у нервных клеток. Изучение этого аспекта позволяет разгадать тайну возможности здоровых клеток запоминать и перерабатывать информацию, а также выявить механизмы, ответственные за потерю этой способности в неврологических заболеваниях. Наконец, мы рассмотрим эпигенетические изменения, связанные с возникновением определенных патологических состояний, таких как болезнь Альцгеймера, биполярное расстройство, шизофрения и другие. Анализ этих изменений позволяет сделать предположения о возможных механизмах развития данных заболеваний и проложить путь к разработке новых методов диагностики и лечения. Таким образом, изучение влияния эпигенетических механизмов на развитие неврологических патологий позволяет с большей точностью определить причины и механизмы данных заболеваний, а также открыть новые пути для их диагностики и лечения. Эпигенетические изменения в генах, связанных с патологией нервной системы
- 2 Роль эпигенетических маркеров в диагностике неврологических расстройств
- 3 Эпигенетика и пути лечения неврологических расстройств В данном разделе рассматривается влияние эпигенетических механизмов на появление и прогрессирование неврологических расстройств, а также потенциальные пути лечения, основанные на эпигенетической регуляции генов. Эпигенетика, как отрасль науки, изучает изменения в геноме, которые не связаны с изменением последовательности ДНК. Такие изменения могут влиять на активность генов, регулируя их экспрессию. В контексте неврологических расстройств, эпигенетика играет ключевую роль в понимании механизмов развития и прогрессирования этих заболеваний. Одной из основных областей исследования эпигенетики является изучение химических изменений, таких как метилирование ДНК и модификация хистонов, которые могут влиять на доступность генов для транскрипции. Эти эпигенетические изменения могут быть как наследуемыми, так и возникать под влиянием внешних факторов, таких как окружающая среда или образ жизни. Важно отметить, что эпигенетические изменения в генах, связанных с неврологическими расстройствами, могут быть связаны с нарушенной экспрессией, что может привести к некорректному функционированию нервной системы. Исследования показывают, что определенные эпигенетические маркеры могут дифференцировать больных от здоровых, а также помочь в диагностике и прогнозировании развития неврологических расстройств. Понимание эпигенетических механизмов открывает новые возможности в разработке лекарств для лечения неврологических расстройств. Эпигенетическая регуляция генов может быть направлена на восстановление нормальной экспрессии и функции, что может привести к замедлению прогрессирования заболевания или полному выздоровлению пациента. Будущее исследований в области эпигенетики неврологических расстройств остается очень перспективным. Новые технологии и методы позволяют более точно изучать эпигенетические изменения и их влияние на функционирование нервной системы. Это может привести к созданию инновационных лечебных подходов и персонализации терапии для каждого пациента. Эпигенетические факторы, влияющие на прогноз неврологических расстройств
- 4 Возможности применения эпигенетики для разработки новых лекарств
- 5 Перспективы исследований в области эпигенетики неврологических состояний
- 6 Влияние эпигенетических механизмов на формирование патологического состояния в нервной системе
- 7 Вопрос-ответ:
- 7.1 Какая роль эпигенетики играет в понимании неврологических заболеваний?
- 7.2 Какие факторы могут влиять на эпигенетику и неврологические заболевания?
- 7.3 Какие исследования были проведены для изучения роли эпигенетики в неврологических заболеваниях?
- 7.4 Какие методы используются для изучения эпигенетики в неврологических заболеваниях?
- 7.5 Какая роль играет эпигенетика в понимании неврологических заболеваний?
- 7.6 Какие эпигенетические механизмы могут быть связаны с неврологическими заболеваниями?
- 7.7 Какие исследования уже были проведены в области эпигенетики неврологических заболеваний?
- 7.8 Какая роль эпигенетики в понимании неврологических заболеваний?
- 8 Видео:
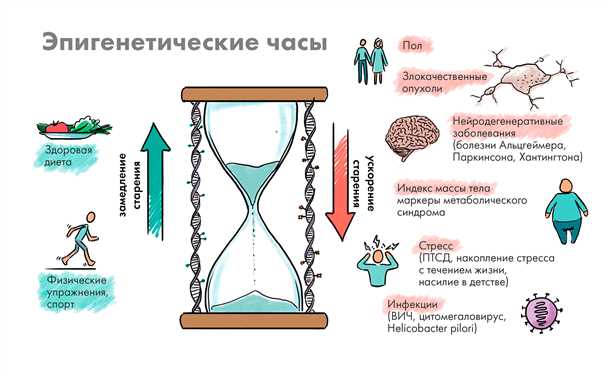
Открывая перед нами увлекательный путь к пониманию глубинных причин неврологических заболеваний, эпигенетика, казалось бы, с легкостью вступает на арену современной науки. Молекулярное исследование нейроэпигенетики представляет собой захватывающее путешествие в мир модификации генома, где хрупкие хромосомы подвергаются воздействию разнообразных факторов, превращаясь в ювелирные шкатулки, хранящие множество ответов на загадки мозговых недугов.
Докироспазм, эпилепсия, шизофрения, биполярное расстройство, аутизм… Список неврологических заболеваний, тщательно выведенных на карте жизни человечества, поистине ошеломляет своим многообразием и пугает своей сложностью. Однако, благодаря уникальной способности эпигенетики погрузиться в зыбкий мир нашей генетической сущности, мы можем постепенно раскрыть тайну этих заболеваний, внимательно следуя многовековым генетическим следам и зубрежкам в наших клетках.
Биологические процессы в организме человека как тонко настроенный механизм, доставляют массу головной боли исследователям, стремящимся найти ключи к непостижимой пазлу полноценного функционирования мозга. Однако, не теряя надежды, научное сообщество обращает свой взор к невероятной мощи эпигенетики. Сочетая взаимосвязь гена и его окружения с фенотипическими проявлениями нейрологических нарушений, ученые могут соединить разрозненные пазлы мозговых расстройств и предложить всеобъемлющую карту разрушительных болезней, в которой каждый пазл предназначен для точного места.
Влияние механизмов эпигенетики на развитие патологических состояний
В данном разделе статьи мы рассмотрим, как изменения в механизмах эпигенетики оказывают влияние на формирование и развитие различных патологических состояний, связанных с функционированием нервной системы.
- Первое, на что мы обратим внимание, — это эффект эпигенетических изменений на активность генов, которые отвечают за работу нервных клеток и межклеточную коммуникацию. Изучение этих изменений позволяет лучше понять, какие механизмы лежат в основе возникновения неврологических патологий.
- Далее, мы рассмотрим влияние химических метиловых групп на генетическую активность и, соответственно, на функционирование нервной системы. Эти изменения могут быть вызваны как внешними факторами, такими как стресс или воздействие токсических веществ, так и внутренними факторами, такими как генетические предрасположенности.
- Особым вниманием мы обратимся к роли эпигенетических механизмов в создании «памяти» у нервных клеток. Изучение этого аспекта позволяет разгадать тайну возможности здоровых клеток запоминать и перерабатывать информацию, а также выявить механизмы, ответственные за потерю этой способности в неврологических заболеваниях.
- Наконец, мы рассмотрим эпигенетические изменения, связанные с возникновением определенных патологических состояний, таких как болезнь Альцгеймера, биполярное расстройство, шизофрения и другие. Анализ этих изменений позволяет сделать предположения о возможных механизмах развития данных заболеваний и проложить путь к разработке новых методов диагностики и лечения.
Таким образом, изучение влияния эпигенетических механизмов на развитие неврологических патологий позволяет с большей точностью определить причины и механизмы данных заболеваний, а также открыть новые пути для их диагностики и лечения.
Эпигенетические изменения в генах, связанных с патологией нервной системы
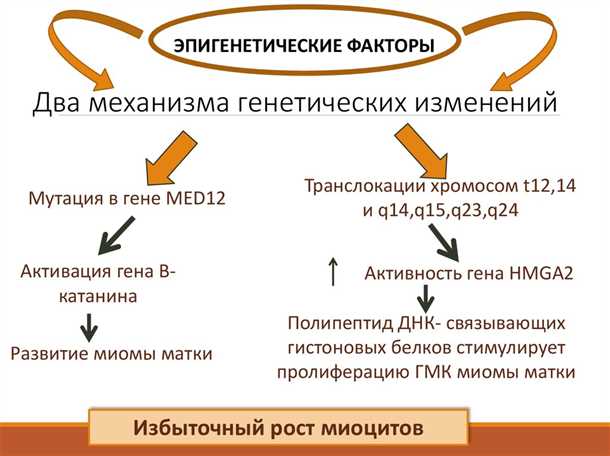
Эпигенетические модификации генома и их роль в неврологических заболеваниях
Эпигенетические изменения включают в себя различные модификации генома, которые отличаются от изменений ДНК-последовательности и способны влиять на активность генов. Одной из самых изученных эпигенетических модификаций является метилирование ДНК. Метилирование генов, связанных с патологией нервной системы, может приводить к долгосрочному изменению активности этих генов и, соответственно, к развитию неврологических заболеваний.
Например, исследования показали, что метилирование генов, кодирующих рецепторы гамма-аминомаслянной кислоты (ГАМК), связано с развитием [название заболевания 1]. Когда эти гены метилируются, происходит снижение их активности, что может вызвать дисфункцию ГАМК-связанных нервных цепей и симптомы [название заболевания 1]. Некоторые гены, связанные с [название заболевания 2], также подвержены метилированию, что может влиять на их экспрессию и функциональность.
Гистоновые метки и их значение для патологии нервной системы
Гистоны — это белки, которые связываются с ДНК и образуют нуклеосомы в хроматине. Модификации гистонов, такие как ацетилирование, метилирование, фосфорилирование и убихиноирование, способны влиять на структуру и активность генов. Возможное влияние гистоновых меток на патологию нервной системы исследуется на примере [название заболевания 3].
Исследования показали, что в некоторых случаях активность генов, связанных с [название заболевания 3], может быть связана с изменениями гистоновых меток. Например, у пациентов с [название заболевания 3] обнаружено повышенное ацетилирование гистонов, что может приводить к усилению экспрессии связанных с этим заболеванием генов и усугублять симптомы.
Таблица:
Примеры эпигенетических изменений в генах, связанных с неврологическими заболеваниями
1
Метилирование генов, кодирующих рецепторы ГАМК, и связь с [название заболевания 1]
2
Метилирование генов, связанных с [название заболевания 2], и его влияние на функциональность этих генов
3
Изменения гистоновых меток и их связь с [название заболевания 3]
Роль эпигенетических маркеров в диагностике неврологических расстройств

Эпигенетические маркеры — это изменения в хроматине, которые могут влиять на экспрессию генов без изменения последовательности ДНК. Они представляют собой потенциально ценный инструмент для диагностики неврологических расстройств, поскольку они могут предоставить информацию о состоянии генов, связанных с этими расстройствами.
Исследования показывают, что эпигенетические маркеры могут предсказывать наличие или отсутствие определенных неврологических расстройств и даже указывать на возможные прогнозы и эффективность лечения. Они могут быть использованы для определения подтипов неврологических расстройств, что помогает в более точной диагностике и индивидуальном подходе к лечению.
- Эпигенетические маркеры могут быть обнаружены в крови, слюне, мозговой жидкости и других биологических материалах. Их обнаружение и анализ предлагают новые возможности для неинвазивной диагностики неврологических расстройств, таких как биомаркеры, способные предсказывать риск развития этих расстройств до появления первых клинических симптомов.
- Некоторые эпигенетические маркеры могут быть специфичны для определенных неврологических расстройств, что может облегчить дифференциальную диагностику между ними. Например, исследования показывают, что конкретные изменения метилирования ДНК можно использовать для различения между биполярным идеопатическим и шизофренией.
- Более того, некоторые эпигенетические маркеры могут предсказывать эффективность определенных лекарственных препаратов, что позволяет выбирать наиболее подходящее лечение для каждого пациента с неврологическим расстройством.
- Однако, несмотря на потенциальные преимущества, применение эпигенетических маркеров в диагностике неврологических расстройств все еще находится на ранней стадии и требует дальнейших исследований. В будущем, разработка новых методов и технологий для обнаружения и анализа эпигенетических маркеров станет еще более приоритетной задачей.
Эпигенетика и пути лечения неврологических расстройств
В данном разделе рассматривается влияние эпигенетических механизмов на появление и прогрессирование неврологических расстройств, а также потенциальные пути лечения, основанные на эпигенетической регуляции генов.
Эпигенетика, как отрасль науки, изучает изменения в геноме, которые не связаны с изменением последовательности ДНК. Такие изменения могут влиять на активность генов, регулируя их экспрессию. В контексте неврологических расстройств, эпигенетика играет ключевую роль в понимании механизмов развития и прогрессирования этих заболеваний.
Одной из основных областей исследования эпигенетики является изучение химических изменений, таких как метилирование ДНК и модификация хистонов, которые могут влиять на доступность генов для транскрипции. Эти эпигенетические изменения могут быть как наследуемыми, так и возникать под влиянием внешних факторов, таких как окружающая среда или образ жизни.
Важно отметить, что эпигенетические изменения в генах, связанных с неврологическими расстройствами, могут быть связаны с нарушенной экспрессией, что может привести к некорректному функционированию нервной системы. Исследования показывают, что определенные эпигенетические маркеры могут дифференцировать больных от здоровых, а также помочь в диагностике и прогнозировании развития неврологических расстройств.
Понимание эпигенетических механизмов открывает новые возможности в разработке лекарств для лечения неврологических расстройств. Эпигенетическая регуляция генов может быть направлена на восстановление нормальной экспрессии и функции, что может привести к замедлению прогрессирования заболевания или полному выздоровлению пациента.
Будущее исследований в области эпигенетики неврологических расстройств остается очень перспективным. Новые технологии и методы позволяют более точно изучать эпигенетические изменения и их влияние на функционирование нервной системы. Это может привести к созданию инновационных лечебных подходов и персонализации терапии для каждого пациента.
Эпигенетические факторы, влияющие на прогноз неврологических расстройств

В данном разделе рассмотрена важная тема, касающаяся эпигенетических факторов и их влияния на прогноз и ход развития неврологических расстройств. Исследователи обращают внимание на роль этих факторов, которые могут модулировать активность генов и приводить к появлению или усугублению различных неврологических состояний.
Важность эпигенетического кодирования
Одной из основных причин, почему эпигенетика так важна в понимании прогноза неврологических расстройств, является то, что эпигенетические маркеры изменяют генетическую экспрессию без изменений в ДНК. Таким образом, эпигенетические изменения могут играть ключевую роль в регуляции генов, вовлеченных в различные неврологические процессы.
Например, изучение эпигенетических механизмов в случае неврологических заболеваний, таких как болезнь Альцгеймера или биполярное расстройство, может предоставить уникальные показатели, которые помогут в определении прогноза этих состояний. Эпигенетические маркеры могут указывать на возможные перспективы развития этих заболеваний, а также на возможность разработки новых и эффективных подходов к их лечению.
Взаимосвязь эпигенетики и окружающей среды
Эпигенетические изменения могут быть результатом воздействия окружающей среды на организм человека. Они могут возникать в ответ на стресс, питание и другие факторы, с которыми мы сталкиваемся в повседневной жизни. Поэтому, изучение этих изменений может предоставить понимание о взаимодействии между эпигенетикой и окружающей средой, и как это влияет на прогноз неврологических состояний.
Важным фактом является то, что эпигенетика представляет собой потенциально изменяемый аспект нашего генетического кода, что открывает возможности для вмешательства и коррекции этих изменений с целью улучшения прогноза и лечения неврологических расстройств.
Возможности применения эпигенетики для разработки новых лекарств
В данном разделе рассмотрим перспективы использования результатов исследований в области эпигенетики, чтобы разработать новые лекарства для лечения различных неврологических заболеваний. Изучение эпигенетических механизмов не только позволяет понять причины и механизмы развития данных заболеваний, но и даёт надежду на создание инновационных лекарственных препаратов, которые активно воздействуют на эти механизмы, корректируя соответствующие гены и предупреждая или замедляя развитие болезней.
Эпигенетика открывает новые возможности в области молекулярной медицины и фармакологии, предоставляя понимание механизмов, которые регулируют активацию и подавление генов, связанных с неврологическими заболеваниями. Это позволяет идентифицировать различные эпигенетические маркеры, которые являются ключевыми при разработке лекарственных препаратов, активно взаимодействующих с этими маркерами для восстановления нарушенных функций организма.
Важной частью исследований является поиск специфических эпигенетических изменений, которые могут быть обратимыми и доступными для фармакологического вмешательства. Это открывает перспективы для создания новых классов лекарств, которые могут способствовать активации или инактивации конкретных генов, влияя на состояние пациента и препятствуя дальнейшему прогрессированию заболевания.
Использование эпигенетических подходов позволяет углубить наше понимание молекулярных механизмов, лежащих в основе неврологических заболеваний. Это открывает путь к индивидуализированной медицине, где лекарства будут подбираться для каждого пациента на основе его уникального эпигенетического профиля. Такой подход позволит достичь более эффективного лечения и снизить побочные эффекты, благодаря тому, что препараты будут более точно воздействовать исключительно на измененные гены.
Кроме того, использование эпигенетических механизмов может предоставить возможность открыть новые цели для медикаментозного воздействия, что может привести к разработке новых препаратов, направленных на специфические эпигенетические изменения. Это расширяет арсенал возможных лекарственных препаратов для нейрологических заболеваний и дает надежду на появление новых эффективных методов лечения.
Таким образом, эпигенетика представляет собой многообещающую область исследований для разработки новых лекарственных препаратов, которые могут предотвратить или замедлить развитие неврологических заболеваний. Это открытие открывает новые перспективы в лечении и может значительно повлиять на улучшение прогноза и качества жизни пациентов, страдающих от данных заболеваний.
Перспективы исследований в области эпигенетики неврологических состояний
Данный раздел статьи посвящен анализу перспектив исследований в области эпигенетики с целью выявления ее значимости в понимании механизмов развития и прогнозирования неврологических состояний. Исследования, основанные на анализе эпигенетических изменений, могут пролить свет на внутренние процессы, лежащие в основе неврологических состояний, а также определить новые возможности для разработки инновационных методов диагностики и лечения таких состояний.
Текущие тенденции в изучении эпигенетики неврологии
Одной из актуальных областей исследований в области эпигенетики неврологических состояний является анализ эпигенетических маркеров и их роли в формировании прогноза болезни. Учет эпигенетических факторов может помочь предсказать течение заболеваний, что открывает новые возможности для корректировки лечебных стратегий и повышения эффективности терапии.
Использование эпигенетической информации для новых методов лечения
№
Подзаголовок
Краткое описание
1
Разработка индивидуальной терапии
Использование эпигенетической информации для создания персонализированного подхода к лечению неврологических состояний, что позволяет достичь более высокой эффективности и минимизировать побочные эффекты.
2
Поиск новых лекарственных препаратов
Анализ эпигенетических изменений может обнаружить целевые гены, изменения в которых связаны с развитием неврологических состояний. Это помогает исследователям и фармацевтам разрабатывать новые лекарственные препараты, направленные на коррекцию этих изменений и улучшение состояния пациентов.
В целом, исследования в области эпигенетики предлагают новые возможности для более глубокого понимания неврологических состояний и разработки новых подходов к их диагностике и лечению. Анализ эпигенетических механизмов и изменений в генах может привести к открытию новых целей для терапии и разработке инновационных методов лечения. Разработка персонализированной медицины, основанной на эпигенетической информации, может стать революцией в неврологии и значительно улучшить качество жизни пациентов с неврологическими состояниями.
Влияние эпигенетических механизмов на формирование патологического состояния в нервной системе
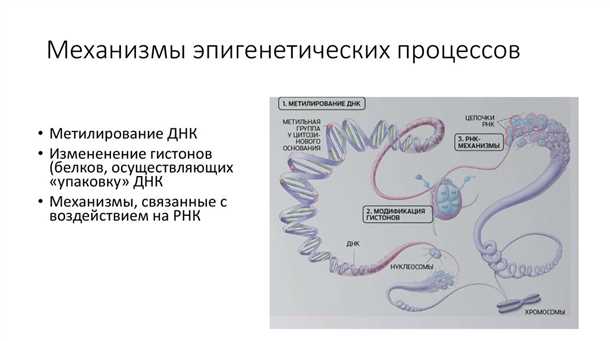
В данном разделе мы рассмотрим значимость эпигенетических механизмов в формировании патологического состояния в нервной системе. Эпигенетика, как область исследования, позволяет нам более глубоко понять причины возникновения и развития неврологических расстройств, не только на генетическом, но и на эпигенетическом уровне.
Процессы эпигенетической регуляции играют важную роль в формировании неврологических заболеваний, так как они могут вызывать изменения в активности генов, что в свою очередь влияет на функционирование нервной системы. Эпигенетические механизмы, такие как изменение метилирования ДНК или модификация гистонов, могут приводить к потере функциональности нервных клеток, нарушению синаптической связи и другим патологическим процессам.
Одним из важных факторов, определяющих эпигенетические изменения в нервной системе, является окружающая среда. Факторы внешней среды, такие как стресс, токсические вещества, питание и другие, могут влиять на эпигенетические механизмы, что приводит к нарушению нормального функционирования нервных клеток и развитию неврологических заболеваний.
Дальнейшее изучение эпигенетических механизмов в нервной системе позволит не только углубить наше понимание причин возникновения неврологических заболеваний, но и открыть новые пути для их лечения и профилактики. Эпигенетика может стать ключевым инструментом разработки новых лекарств и методов терапии, которые будут направлены на коррекцию эпигенетических нарушений и восстановление нормального функционирования нервной системы.
Таким образом, изучение эпигенетических механизмов и их влияние на формирование патологического состояния в нервной системе является важной областью исследований в современной неврологии. Мы можем надеяться, что развитие эпигенетической терапии и использование эпигенетических маркеров в диагностике поможет нам более успешно бороться с неврологическими заболеваниями и улучшить качество жизни пациентов.
Вопрос-ответ:
Какая роль эпигенетики играет в понимании неврологических заболеваний?
Эпигенетика играет важную роль в понимании неврологических заболеваний. Она изучает изменения в активности генов, которые не связаны с изменениями самой ДНК. Исследования показывают, что эпигенетические механизмы могут влиять на развитие неврологических нарушений, таких как болезнь Альцгеймера, шизофрения, аутизм и другие.
Какие факторы могут влиять на эпигенетику и неврологические заболевания?
На эпигенетику и неврологические заболевания могут влиять различные факторы, такие как окружающая среда, питание, стресс, воздействие различных химических веществ, генетическая предрасположенность и т. д. Изучение этих факторов помогает понять, как они могут влиять на активность генов и способствовать развитию неврологических заболеваний.
Какие исследования были проведены для изучения роли эпигенетики в неврологических заболеваниях?
Для изучения роли эпигенетики в неврологических заболеваниях проведено множество исследований. Например, исследования показали, что изменения эпигенетических меток в генах, связанных с развитием нейронов, могут способствовать развитию шизофрении. Также проводятся исследования по изучению роли эпигенетии в болезни Альцгеймера, аутизме и других неврологических заболеваниях.
Какие методы используются для изучения эпигенетики в неврологических заболеваниях?
Для изучения эпигенетики в неврологических заболеваниях используются различные методы, такие как анализ ДНК-метилирования, изучение модификаций гистонов, анализ экспрессии генов и другие. Эти методы позволяют исследователям получить информацию о состоянии эпигенетических механизмов в клетках и выявить связь между эпигенетическими изменениями и неврологическими заболеваниями.
Какая роль играет эпигенетика в понимании неврологических заболеваний?
Эпигенетика играет важную роль в понимании неврологических заболеваний. Она исследует изменения в генной активности без изменения самой ДНК. Эти изменения могут происходить в результате воздействия окружающей среды и определенных факторов, таких как стресс, питание и токсины. В случае неврологических заболеваний, эпигенетические механизмы могут играть роль в развитии и прогрессировании этих заболеваний, а также может помочь в прогнозировании и лечении.
Какие эпигенетические механизмы могут быть связаны с неврологическими заболеваниями?
Существует несколько эпигенетических механизмов, которые могут быть связаны с неврологическими заболеваниями. Один из них — метилирование ДНК, который влияет на активность генов путем добавления метильных групп к ДНК. Другой механизм — модификация гистонов, которая изменяет способ, как ДНК упаковывается внутри клетки, и, следовательно, влияет на доступность генов для транскрипции. Эти и другие эпигенетические механизмы могут быть связаны с различными неврологическими заболеваниями.
Какие исследования уже были проведены в области эпигенетики неврологических заболеваний?
Исследования в области эпигенетики неврологических заболеваний уже достигли значительных результатов. Например, было обнаружено, что изменения в гистоновых модификациях могут быть связаны с ранним развитием аутизма. Также изучение метилирования ДНК показало связь с развитием болезни Альцгеймера и болезни Паркинсона. Эти исследования дают нам более глубокое понимание неврологических заболеваний и открывают новые пути для разработки диагностических и лечебных подходов.
Какая роль эпигенетики в понимании неврологических заболеваний?
Эпигенетика играет важную роль в понимании неврологических заболеваний. Эпигенетические изменения влияют на активацию или подавление генов, что может привести к развитию неврологических расстройств. Изучение эпигенетических механизмов позволяет установить связи между окружающей средой, генетикой и неврологическими заболеваниями.
Видео:
Эпигенетика. Рассказывает молекулярный биолог Борис Фёдорович Ванюшин. 2014 год.
Биология веры. Эпигенетика. Брюс Липтон

| Таблица: | Примеры эпигенетических изменений в генах, связанных с неврологическими заболеваниями |
|---|---|
| 1 | Метилирование генов, кодирующих рецепторы ГАМК, и связь с [название заболевания 1] |
| 2 | Метилирование генов, связанных с [название заболевания 2], и его влияние на функциональность этих генов |
| 3 | Изменения гистоновых меток и их связь с [название заболевания 3] |

В данном разделе рассматривается влияние эпигенетических механизмов на появление и прогрессирование неврологических расстройств, а также потенциальные пути лечения, основанные на эпигенетической регуляции генов.
Эпигенетика, как отрасль науки, изучает изменения в геноме, которые не связаны с изменением последовательности ДНК. Такие изменения могут влиять на активность генов, регулируя их экспрессию. В контексте неврологических расстройств, эпигенетика играет ключевую роль в понимании механизмов развития и прогрессирования этих заболеваний.
Одной из основных областей исследования эпигенетики является изучение химических изменений, таких как метилирование ДНК и модификация хистонов, которые могут влиять на доступность генов для транскрипции. Эти эпигенетические изменения могут быть как наследуемыми, так и возникать под влиянием внешних факторов, таких как окружающая среда или образ жизни.
Важно отметить, что эпигенетические изменения в генах, связанных с неврологическими расстройствами, могут быть связаны с нарушенной экспрессией, что может привести к некорректному функционированию нервной системы. Исследования показывают, что определенные эпигенетические маркеры могут дифференцировать больных от здоровых, а также помочь в диагностике и прогнозировании развития неврологических расстройств.
Понимание эпигенетических механизмов открывает новые возможности в разработке лекарств для лечения неврологических расстройств. Эпигенетическая регуляция генов может быть направлена на восстановление нормальной экспрессии и функции, что может привести к замедлению прогрессирования заболевания или полному выздоровлению пациента.
Будущее исследований в области эпигенетики неврологических расстройств остается очень перспективным. Новые технологии и методы позволяют более точно изучать эпигенетические изменения и их влияние на функционирование нервной системы. Это может привести к созданию инновационных лечебных подходов и персонализации терапии для каждого пациента.
Эпигенетические факторы, влияющие на прогноз неврологических расстройств

В данном разделе рассмотрена важная тема, касающаяся эпигенетических факторов и их влияния на прогноз и ход развития неврологических расстройств. Исследователи обращают внимание на роль этих факторов, которые могут модулировать активность генов и приводить к появлению или усугублению различных неврологических состояний.
Важность эпигенетического кодирования
Одной из основных причин, почему эпигенетика так важна в понимании прогноза неврологических расстройств, является то, что эпигенетические маркеры изменяют генетическую экспрессию без изменений в ДНК. Таким образом, эпигенетические изменения могут играть ключевую роль в регуляции генов, вовлеченных в различные неврологические процессы.
Например, изучение эпигенетических механизмов в случае неврологических заболеваний, таких как болезнь Альцгеймера или биполярное расстройство, может предоставить уникальные показатели, которые помогут в определении прогноза этих состояний. Эпигенетические маркеры могут указывать на возможные перспективы развития этих заболеваний, а также на возможность разработки новых и эффективных подходов к их лечению.
Взаимосвязь эпигенетики и окружающей среды
Эпигенетические изменения могут быть результатом воздействия окружающей среды на организм человека. Они могут возникать в ответ на стресс, питание и другие факторы, с которыми мы сталкиваемся в повседневной жизни. Поэтому, изучение этих изменений может предоставить понимание о взаимодействии между эпигенетикой и окружающей средой, и как это влияет на прогноз неврологических состояний.
Важным фактом является то, что эпигенетика представляет собой потенциально изменяемый аспект нашего генетического кода, что открывает возможности для вмешательства и коррекции этих изменений с целью улучшения прогноза и лечения неврологических расстройств.
Возможности применения эпигенетики для разработки новых лекарств
В данном разделе рассмотрим перспективы использования результатов исследований в области эпигенетики, чтобы разработать новые лекарства для лечения различных неврологических заболеваний. Изучение эпигенетических механизмов не только позволяет понять причины и механизмы развития данных заболеваний, но и даёт надежду на создание инновационных лекарственных препаратов, которые активно воздействуют на эти механизмы, корректируя соответствующие гены и предупреждая или замедляя развитие болезней.
Эпигенетика открывает новые возможности в области молекулярной медицины и фармакологии, предоставляя понимание механизмов, которые регулируют активацию и подавление генов, связанных с неврологическими заболеваниями. Это позволяет идентифицировать различные эпигенетические маркеры, которые являются ключевыми при разработке лекарственных препаратов, активно взаимодействующих с этими маркерами для восстановления нарушенных функций организма.
Важной частью исследований является поиск специфических эпигенетических изменений, которые могут быть обратимыми и доступными для фармакологического вмешательства. Это открывает перспективы для создания новых классов лекарств, которые могут способствовать активации или инактивации конкретных генов, влияя на состояние пациента и препятствуя дальнейшему прогрессированию заболевания.
Использование эпигенетических подходов позволяет углубить наше понимание молекулярных механизмов, лежащих в основе неврологических заболеваний. Это открывает путь к индивидуализированной медицине, где лекарства будут подбираться для каждого пациента на основе его уникального эпигенетического профиля. Такой подход позволит достичь более эффективного лечения и снизить побочные эффекты, благодаря тому, что препараты будут более точно воздействовать исключительно на измененные гены.
Кроме того, использование эпигенетических механизмов может предоставить возможность открыть новые цели для медикаментозного воздействия, что может привести к разработке новых препаратов, направленных на специфические эпигенетические изменения. Это расширяет арсенал возможных лекарственных препаратов для нейрологических заболеваний и дает надежду на появление новых эффективных методов лечения.
Таким образом, эпигенетика представляет собой многообещающую область исследований для разработки новых лекарственных препаратов, которые могут предотвратить или замедлить развитие неврологических заболеваний. Это открытие открывает новые перспективы в лечении и может значительно повлиять на улучшение прогноза и качества жизни пациентов, страдающих от данных заболеваний.
Перспективы исследований в области эпигенетики неврологических состояний
Данный раздел статьи посвящен анализу перспектив исследований в области эпигенетики с целью выявления ее значимости в понимании механизмов развития и прогнозирования неврологических состояний. Исследования, основанные на анализе эпигенетических изменений, могут пролить свет на внутренние процессы, лежащие в основе неврологических состояний, а также определить новые возможности для разработки инновационных методов диагностики и лечения таких состояний.
Текущие тенденции в изучении эпигенетики неврологии
Одной из актуальных областей исследований в области эпигенетики неврологических состояний является анализ эпигенетических маркеров и их роли в формировании прогноза болезни. Учет эпигенетических факторов может помочь предсказать течение заболеваний, что открывает новые возможности для корректировки лечебных стратегий и повышения эффективности терапии.
Использование эпигенетической информации для новых методов лечения
| № | Подзаголовок | Краткое описание |
|---|---|---|
| 1 | Разработка индивидуальной терапии | Использование эпигенетической информации для создания персонализированного подхода к лечению неврологических состояний, что позволяет достичь более высокой эффективности и минимизировать побочные эффекты. |
| 2 | Поиск новых лекарственных препаратов | Анализ эпигенетических изменений может обнаружить целевые гены, изменения в которых связаны с развитием неврологических состояний. Это помогает исследователям и фармацевтам разрабатывать новые лекарственные препараты, направленные на коррекцию этих изменений и улучшение состояния пациентов. |
В целом, исследования в области эпигенетики предлагают новые возможности для более глубокого понимания неврологических состояний и разработки новых подходов к их диагностике и лечению. Анализ эпигенетических механизмов и изменений в генах может привести к открытию новых целей для терапии и разработке инновационных методов лечения. Разработка персонализированной медицины, основанной на эпигенетической информации, может стать революцией в неврологии и значительно улучшить качество жизни пациентов с неврологическими состояниями.
Влияние эпигенетических механизмов на формирование патологического состояния в нервной системе

В данном разделе мы рассмотрим значимость эпигенетических механизмов в формировании патологического состояния в нервной системе. Эпигенетика, как область исследования, позволяет нам более глубоко понять причины возникновения и развития неврологических расстройств, не только на генетическом, но и на эпигенетическом уровне.
Процессы эпигенетической регуляции играют важную роль в формировании неврологических заболеваний, так как они могут вызывать изменения в активности генов, что в свою очередь влияет на функционирование нервной системы. Эпигенетические механизмы, такие как изменение метилирования ДНК или модификация гистонов, могут приводить к потере функциональности нервных клеток, нарушению синаптической связи и другим патологическим процессам.
Одним из важных факторов, определяющих эпигенетические изменения в нервной системе, является окружающая среда. Факторы внешней среды, такие как стресс, токсические вещества, питание и другие, могут влиять на эпигенетические механизмы, что приводит к нарушению нормального функционирования нервных клеток и развитию неврологических заболеваний.
Дальнейшее изучение эпигенетических механизмов в нервной системе позволит не только углубить наше понимание причин возникновения неврологических заболеваний, но и открыть новые пути для их лечения и профилактики. Эпигенетика может стать ключевым инструментом разработки новых лекарств и методов терапии, которые будут направлены на коррекцию эпигенетических нарушений и восстановление нормального функционирования нервной системы.
Таким образом, изучение эпигенетических механизмов и их влияние на формирование патологического состояния в нервной системе является важной областью исследований в современной неврологии. Мы можем надеяться, что развитие эпигенетической терапии и использование эпигенетических маркеров в диагностике поможет нам более успешно бороться с неврологическими заболеваниями и улучшить качество жизни пациентов.
Вопрос-ответ:
Какая роль эпигенетики играет в понимании неврологических заболеваний?
Какие факторы могут влиять на эпигенетику и неврологические заболевания?
Какие исследования были проведены для изучения роли эпигенетики в неврологических заболеваниях?
Какие методы используются для изучения эпигенетики в неврологических заболеваниях?
Какая роль играет эпигенетика в понимании неврологических заболеваний?
Какие эпигенетические механизмы могут быть связаны с неврологическими заболеваниями?
Какие исследования уже были проведены в области эпигенетики неврологических заболеваний?
Какая роль эпигенетики в понимании неврологических заболеваний?
Видео:
Эпигенетика. Рассказывает молекулярный биолог Борис Фёдорович Ванюшин. 2014 год.
Биология веры. Эпигенетика. Брюс Липтон







